周选择综合测试(四)
1. 人类正面临着石油短缺、油价上涨的难点。下列解决能源问题的办法不当的是( )
A.鼓励个体企业加快煤炭的开采 B.研究和开发借助太阳能
C.建造水电站开发水利资源 D.开发种植可再生能源
2.放射性同位素 ![]() 的原子核内的中子数是
的原子核内的中子数是
A.233 B.67 | C.99 | D.166 |
|
3.下列物质是共价化合物的是 |
|
| |
A.苛性钠 B.硫酸 | C.食盐 | D.氯气 |
|
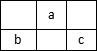 4.a、b、c 均为短周期元素,它们在周期表中的地方如图所示,b 是地壳中含量最多的金属元素,则 a、b、c 分别是
4.a、b、c 均为短周期元素,它们在周期表中的地方如图所示,b 是地壳中含量最多的金属元素,则 a、b、c 分别是
A.C、Al、P B.N、Mg、S C.O、P、Cl D.O、Cl、P
5.下述关于烃的说法中,正确的是
A.烃是指仅含有碳和氢两种元素的有机物 B.烃是指分子里含碳元素的化合物
C.烃是指燃烧反应后生成二氧化碳和水的有机物 D.烃是指含有碳和氢元素的化合物
6.能通过化学反应使溴水褪色,又能使酸性高锰酸钾溶液褪色的是
A.苯 B.四氯化 ![]() C.乙烷 D.乙烯
C.乙烷 D.乙烯
7.炒菜时,加一点酒和醋能使菜味香可口,缘由是
A.有盐类物质生成 B.有酯类物质生成C.有醇类物质生成 D.有酸类物质生成
8.为了确定某物质是不是变质,所选试剂(括号内物质)达不到实验需要的是
A.K2SO3 是不是被氧化(BaCl2) B.FeSO4 是不是被氧化(KSCN)
C.KI 是不是被氧化(淀粉溶液) D.漂粉精是不是被变质(盐酸)
9.沼气是有机废弃物(树叶、草类及垃圾、粪便等)在隔绝空气的条件下发酵分解而成的气体,主要成分是甲烷。农村沼气池中发酵后的池底剩余物是非常不错的沤肥。下面有关结论中,错误的是( )
A.沼气是一种清洗的能源 B.用沼气作能源可以保护森林
C.用沼气的缺点是紧急污染环境 D.用沼气是对化学能的充分借助
10.下列关于浓硫酸的叙述正确的是
A.浓硫酸具备吸水性,因而能使蔗糖炭化 B.浓硫酸在常温下可以使铁、铝等金属钝化
C.浓硫酸是一种干燥剂,可以干燥氨气、氢气等气体
D.浓硫酸在常温下可飞速与铜片反应放出二氧化硫气体
11.用铁片与稀硫酸反应制取氢气时,下列的手段中,不可以使氢气生成速率加快的是
A.加热 B.不需要稀硫酸,改用 98%浓硫酸
C.滴加少量硫酸铜溶液 D.不需要铁片,改用铁粉
12.看出正丁烷和异丁烷互为同分异构体的依据是
A.具备一样的化学性质 B.具备相同的物理性质
C.分子具备相同的空间结构 D.分子式相同,碳原子的空间结构不同
13.大家把食品分为绿色食品、蓝色食品、白色食品等。通过光合用途转化的食品叫绿色食品;海洋提供的食品叫蓝色食品; 通过微生物发酵制得的食品叫白色食品。下列是白色食品的是( )
A.食醋 B.面粉 C.海带 D.菜油
14.工业制硫酸中的一步要紧反应是 SO2 在 400~600 ℃下的催化氧化:
![]() 2SO2+O2 2SO3,这是一个正反应放热的可逆反应。假如反应在密闭容器中进行,下述有关说法中错 误的是
2SO2+O2 2SO3,这是一个正反应放热的可逆反应。假如反应在密闭容器中进行,下述有关说法中错 误的是
A.用催化剂是为了加快反应速率,提升生产效率
B.在上述条件下,SO2 不可能 100%地转化为 SO3
C.为了提升SO2 的实际转化的比例,应适合提升O2 的浓度
D.达到平衡时,SO2 的浓度与 SO3 的浓度相等
15.用氨水、氢氧化钠溶液、盐酸中的任何一种作试剂都能给出辨别的溶液组是
A.Al3 和AgNO3 B .Na2CO3 和NaCl C.Fe23 和 FeCl3 D.NH4Cl 和 MgCl2
16.依据元素周期表和元素周期律剖析下面的判断,其中错误的是
A.铝原子失电子能力比镁弱 B.硫酸的酸性比磷酸强
C.氯化氢比硫化氢稳定 D.氢氧化镁比氢氧化钙的碱性强
17.下列说法中,错误的是
A.人类现在所直接借助的能量大多数是由化学反应产生的
B.煤、石油、天然气是当今世界非常重要的三种化石燃料
C.化学反应中能量变化的大小与反应物的水平多少无关
D.化学反应势必随着发生能量变化,能量变化是化学反应的基本特点之一
18.下列离子在溶液中能很多共存的一组是
A.Na+、Al3+、Cl―、OH― B. Na+、H+、OH―、Cl―
![]() C.NH4 、 Mg 、SO4 、Cl D.Na 、Cl 、HCO3 、H
C.NH4 、 Mg 、SO4 、Cl D.Na 、Cl 、HCO3 、H
 19.下列化学用语的书写,正确的是
19.下列化学用语的书写,正确的是
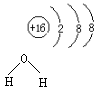
A . 氮气的电子式: ![]() B.硫原子的结构示意图:
B.硫原子的结构示意图:
C . 溴化钠的电子式: ![]() D.水分子的结构式:
D.水分子的结构式:
20.从海水中可以提取溴,但得到的液溴中常溶有少量氯气,除去氯气应该使用的办法是( )
A.加适当的 KI 溶液 B.通入溴蒸气
C.加入适当的NaOH 溶液 D.加入适当的NaBr 溶液
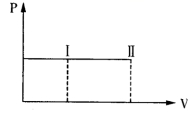 21.一带有活塞的密封容器中盛有A、B 组成的混合气体,在一般条件下,从状况 I 反应到状况 II 时,气体体积(V)与气体压强(P)的变化曲线如图所示。
21.一带有活塞的密封容器中盛有A、B 组成的混合气体,在一般条件下,从状况 I 反应到状况 II 时,气体体积(V)与气体压强(P)的变化曲线如图所示。
![]() 则反应:A+B 2C
则反应:A+B 2C
A.是放热反应 B.反应后气体总分子数增多
C.是吸热反应
D.反应物具备的总能量等于生成物具备的总能量
22.下列反应是取代反应的是
A.甲醛→甲醇 B.乙醛→乙酸 C.乙醇→乙酸乙酯 D. 乙醇→乙烯
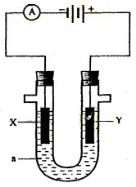 23、右图是电解饱和 NaCl 溶液的实验装置, X、Y 都是惰性电极, a 是饱和 NaCl 溶液, 同时在两边各滴入几滴酚酞试液,下列有关该实验正确的说法是
23、右图是电解饱和 NaCl 溶液的实验装置, X、Y 都是惰性电极, a 是饱和 NaCl 溶液, 同时在两边各滴入几滴酚酞试液,下列有关该实验正确的说法是
A. X 电极为阳极,Y 电极为阴极
B.X 电极溶液变红色, 且有刺激性气味气体产生
C.若将X、Y 两极产生的气体采集起来,其体积比略大于 1:1
D.电解后,将溶液混匀,电解前后溶液的 pH 未发生变化
24.下列做法会致使食品对人体有害的是
①在沥青公路上翻晒粮食 ②香肠中加过量亚硝酸钠以维持肉类新鲜③用无烟煤直接烧烤鸡、鸭 ④用“瘦肉精”喂养生猪
⑤用小苏打做发酵粉制面包 ⑥用乙烯催熟水果
A.①②③⑤ B.①②③④ C.②③④⑤ D.①②③④⑤
25.下列实验中,仪器下端需要插入液面的是
①制备氢气的浅易装置中的长颈漏斗; ②制备氯气装置中的分液漏斗;
③制备 Fe2 操作中的胶头滴管; ④将氯化氢气体溶于水时的导气管;
⑤用乙醇制取乙烯时的温度计; ⑥蒸馏石油时的温度计。
A.①③⑤ B.②④⑥ C.①③④⑤ D.全部
26.下列物质与甲烷肯定互为同系物的是
A.C3H6 B.氯乙烷 C.C5H12 D.环己烷
27.1993 年世纪十大科技新闻称中国学者许志福和美国科学家穆尔一同合成了世界上最大的碳氢分子。一个该分子含 1134 个碳原子和 1146 个氢原子。有关此分子下列说法错误的是( )
A.是烃类化合物 B.常温下为固态 C.具备类似金刚石的硬度 D.易燃烧
28.可用于检验乙醇中是不是含有水的试剂是
A.无水硫酸铜 B.生石灰 C.金属钠 D.胆矾
29.用分液漏斗可以离别的一组混合物是
A.硝基苯和苯 B.乙醇和乙二醇 C.溴苯和水 D.乙酸和水
30、下列有关物质检验的实验结论正确的是( )
| 实 验 操 作 | 现 象 | 实 验 结 论 |
A. | 向某溶液中加入硝酸酸化的氯化钡溶液 | 生成白色沉淀 | 溶液中肯定含有 SO 2- 4 |
B. | 将某气体通入品红溶液中 | 品红溶液褪色 | 该气体肯定是 SO2 |
C. | 往某溶液中加入 KSCN 溶液 | 显血红色 | 溶液中肯定含有 Fe3+ |
D. | 往某溶液中加入盐酸 | 产生无色气体 | 2+ 溶液中肯定含有 CO3 |
31、设 NA 为阿伏加德罗常数的值,下列说法正确的是( )
A.常温常压下,71 g Cl2 含有 2 NA 个Cl 原子
B.把 40 g NaOH 固体溶于 1 L 水中,所得溶液中NaOH 的物质的量浓度为 1 mol·L-1
C.物质的量浓度为 1 mol/L 的 K2SO4 溶液中,含 2 NA 个 K+
D.常温常压下,11.2 L N2 中含有些分子数为 0.5 NA
32、下列物质中,只含有共价键的化合物是 ( )
A.氢氧化钠 B.氯化钠 C.氢气 D.硫化氢
33.下列变化需要加快反应速率的是 ( )
A.合成氨 B.橡胶老化 C.钢铁生锈 D.食物变质
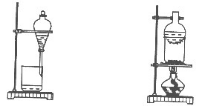
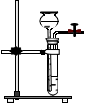 34 下列装置所示的实验中,能达到实验目的的是( )
34 下列装置所示的实验中,能达到实验目的的是( )
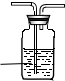 ¾¾N¾O®
¾¾N¾O®
A.离别碘酒中的碘和酒精
B.除去氯化铵中的碘
水 ____________________
C.排水法采集NO
D.检查装置气密性
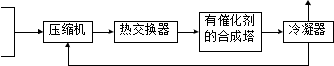
35、工业合成氨的浅易步骤如下:通过循环Ⅰ可借助的气态物质是( )
液氨
 N2
N2
H2
循环Ⅰ
A.催化剂 B.只有N2 C.只有 H2 D.N2 和H2
36、用 0.1000mol/L 盐酸滴定 NaOH 溶液(滴有 2 滴甲基橙)时,终点颜色变化是( )
A.黄色—红色 B.黄色—橙色 C.橙色—黄色 D.红色—橙色
![]() 对于铝热反应:Fe2O3 + 2Al 高温2Fe + Al2O3,下列说法中正确的是 ( )
对于铝热反应:Fe2O3 + 2Al 高温2Fe + Al2O3,下列说法中正确的是 ( )
A.Fe 元素的化合价升高 B.若 27 g Al 参加反应则有 3 mol 电子转移
C.Fe2O3 发生氧化反应 D.Al 被还原
![]() 在肯定条件下,对于密闭容器中进行的可逆反应:2NO2 N2O4 ,下列说法中,能说明这一反应已经达到化学平衡状况的是( )
在肯定条件下,对于密闭容器中进行的可逆反应:2NO2 N2O4 ,下列说法中,能说明这一反应已经达到化学平衡状况的是( )
A.NO2、N2O4 的浓度相等
B.NO2、N2O4 在容器中共存
C.NO2、N2O4 的浓度均不再变化
D.单位时间内消耗 2 mol NO2,同时生成 1 mol N2O4
某原子的最外层上只有一个电子,则它跟氯原子结合时能形成的化学键是( )
A.肯定是共价键 B.肯定是离子键
C.可能是共价键,也会是离子键 D.以上说法均不正确
40.对室温下pH相同、体积相同的醋酸和盐酸两种溶液分别采拿下列手段,有关叙述正确的是( )
A.加适当的醋酸钠晶体后,两溶液的pH均增大
B.使温度都升高20℃后,两溶液的pH均不变
C.加水稀释2倍后,两溶液的pH均减小
D.加足量的锌充分反应后,两溶液中产生的氢气一样多







